РУКОВОДСТВО ПО ВАКЦИНАЦИИ КОШЕК
ИНДИВИДУАЛЬНАЯ ВАКЦИНАЦИЯ КОШЕК
Основной график иммунизации
Базовыми вакцинами для кошек являются вакцины, защищающие
от FPV, FHV-1 и FCV. Примером вакцины, которая может считаться базовой в некоторых странах, является вакцина против вируса бешенства. В географических регионах, где эта инфекция является эндемичным (энзоотичным) заболеванием, группа VGG рекомендует регулярно вакцинировать всех кошек для защиты как популяции домашних животных, так и людей. В некоторых странах обязательная вакцинация против бешенства предусмотрена требованиями законодательства (хотя
они не всегда распространяются на кошек), и, кроме того, вакцинация против бешенства необходима для международных путешествий с питомцами. В том, что касается базовых вакцин для кошек, важно понимать, что защита, которую предоставляют вакцины против FCV и FHV-1, не сопоставима с иммунитетом, который обеспечивают вакцины против FPV. Поэтому от базовых вакцин для кошек против респираторных
болезней не следует ожидать, что они дадут такую же стойкую защиту либо длительность иммунитета, которая наблюдается у базовых вакцин для собак. Вакцины против FCV были разработаны для выработки перекрестного иммунитета против многочисленных штаммов FCV, однако все еще возможны случаи инфицирования и заболевания вакцинированных взрослых животных (Pedersen et al. 2000, Schorr-Evans et al. 2003) [EB1]. Нет вакцины против FHV-1, которая могла бы защитить от заражения вирулентным вирусом, и такое инфицирование может протекать латентно с сохранением возможности реактивации вирулентного вируса в периоды сильного стресса (Richter et al. 2009, Maes 2012) [EB1]. Реактивировавшись, вирус может вызвать появление клинических признаков у вакцинированного животного или будет выделяться и вызывать заболевание у восприимчивых животных. Группа VGG рекомендует ревакцинацию кошек с низким риском заражения против FHV-1 и FCV один раз в три года на основании опубликованного исследования, согласно которому минимальная длительность частичного, но клинически значимого иммунитета для этих базовых вакцин составляет 7,5 лет (Scott & Geissinger 1999). Более позднее исследование МЖВ вакцин против FHV-1/FCV показало, что через 3 года после вакцинации защита против FHV-1 является частичной и намного менее надежна, хотя результаты для частичной защиты от FCV были сопоставимы с результатами, полученными Скоттом (Scott) и Гейзингером (Geissinger) в 1999 году (Jas et al. 2015) [EB1]. Группа VGG рекомендует проводить ежегодную ревакцинацию кошек против FHV-1/FCV в случаях высокого риска заражения. Кошкой, имеющей низкий риск заражения, можно считать животное домашнего содержания, являющееся единственным у
владельцев и не посещающее зоогостиниц. Кошку с высоким риском можно охарактеризовать как животное, которое регулярно бывает в зоогостиницах, либо живет в доме, где содержат несколько
кошек, с возможностью выгула на улице. Более того, группа VGG советует практикующим ветеринарным врачам обдумать сроки введения вакцин против FHV-1/FCV кошкам, подверженным высокому риску, если их регулярно отдают в зоогостиницы. Самый стойкий иммунитет, обеспечиваемый этими вакцинами, приходится на 3-месячный период после вакцинации (Gaskell et al. 2007) [EB1], поэтому, возможно, лучше вводить их кошке, которая регулярно бывает в зоогостинице, непосредственно перед ежегодным размещением в ней.
Необходимость вакцинации против вирусной лейкемии кошек (Feline Leukemia Virus, FeLV) тоже часто вызывает споры среди специалистов. Группа VGG относит вакцину против FeLV к дополнительным, но в полной мере осознает, что ее использование должно определяться стилем жизни и предполагаемыми рисками, которым подвергается конкретная кошка, связаными в том числе с распространенностью данной инфекции в окружающей ее среде. Многие специалисты-фелинологи считают, что, несмотря на значительное снижение частоты встречаемости инфицирования кошек вирусом FeLV во многих частях мира благодаря успешно реализованными программам контроля (Weijer and Daams 1976, Weijer et al. 1986, 1989, Meichner et al. 2012) [EB1], в
географических областях, где вирусная лейкемия по-прежнему широко распространена, любая кошка моложе 1 года, в содержании которой присутствует элемент выгула на улице (даже если она просто содержится вместе с кошкой, которая бывает на улице), должна получить защиту посредством плановой вакцинации двумя дозами вакцины с интервалом 2-4 недели, начиная с возраста не менее 8 недель. Эта оценка соотношения «риск-польза» в отношении FeLV должна стать обычной частью беседы с владельцем, которая проводится при вакцинации кошек, и вакцинировать
следует только FeLV-негативных животных.
Группа VGG также пересмотрела подход к вакцинации против вируса иммунодефицита кошек (Feline Immunodeficiency Virus, FIV), которая в предыдущих версиях этого руководства была отнесена к нерекомендуемым. В основе такой классификации лежали следующие соображения:
(1) сомнения в наличии перекрестной защиты между подтипами вируса, которые вошли в состав вакцины, и его полевыми подтипами и рекомбинантами в различных географических регионах (Hosie et al. 1995, Dunham et al. 2006, Yamamoto et al. 2007, Coleman et al. 2014, Beczkowski et al.
2015a) [EB1],
(2) создание после введения вакцины препятствий для диагностики FIV-инфекции с помощью определения антител (Hosie & Beatty 2007) [EB1], и (3) тот факт, что это адъювантная вакцина, которая должна вводиться неоднократно (первичный курс из трех инъекций и ежегодная ревакцинация) виду животных, предрасположенному к возникновению постинъекционной саркомы. Группе VGG известно, что в некоторых частях мира сохраняется значительная распространенность серопозитивности и/или инфицирования FIV (Bennett et al. 1989, Hosie et al. 1989, Friend et al. 1990, Glennon et al. 1991, Bandecchi et al. 1992, Hitt et al. 1992, Ueland and Lutz
1992, Jones et al. 1995, Hofmann-Lehmann et al. 1996, Yilmaz et al. 2000, Lee et al. 2002, Muirden 2002, Norris et al. 2007, Gleich et al. 2009, Ravi et al. 2010, Bande et al. 2012, Chang Fung Martel et al. 2013, Rypula et al. 2014) [EB1]. Сейчас существуют селективные (дифференцирующие, то есть различающие поствакцинальные антитела и антитела, образовавшиеся в результате естественного заражения) серологические тесты (Kusuhara et al 2007, Levy et al. 2008, Westman et al. 2015) и более надежный ПЦР-анализ для диагностики FIV-инфекции (Arjona et al. 2007, Wang et al. 2010, Morton
et al. 2012) [EB1]. Во многих странах вероятность того, что можно будет убедить владельцев содержать кошек дома, без выгула на улице, оградив их таким образом от основного риска передачи FIV (через укусы инфицированных кошек), довольно низка. Недавно было показано, что на
прогрессирование болезни у FIV-инфицированных кошек оказывают влияние условия проживания и число кошек в семье (Beczkowski et al. 2015b). Принимая во внимание тот факт, что эта вакцина была эффективна в одних исследованиях и не эффективна в других и может быть полезна
некоторым популяциям кошек, подверженным риску заражения, группа VGG изменила классификацию этого препарата, отнеся его к дополнительным вакцинам.
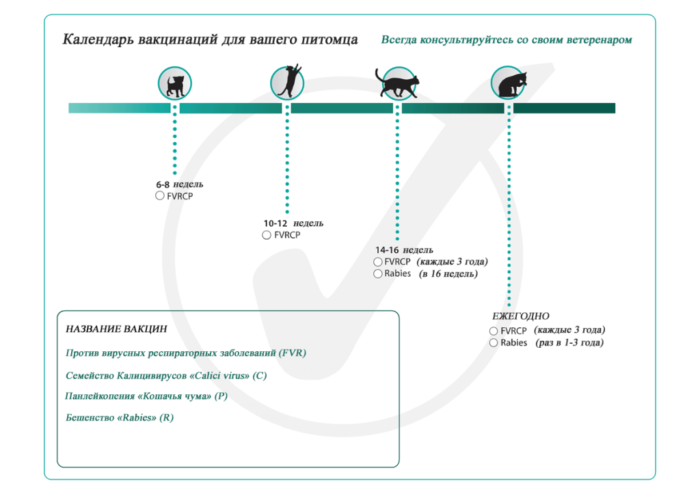
Вакцинация котят и ревакцинация в 6 или 12 месяцев
Как и щенки, большинство котят в первые недели жизни защищены материнскими антителами. Но без серологического тестирования уровень этой защиты и момент, когда котенок утратит защиту от инфекции и сможет иммунологически ответить на вакцинацию, определить нельзя. Это зависит от уровня антител у матери и от количества антител, поглощенных с молозивом котятами из разных пометов и отдельными котятами в каждом помете. Как правило, снижение количества материнских антител до уровня, позволяющего провести активную иммунизацию, происходит к 8-12 неделям; но котята с низким уровнем материнских антител могут быть уязвимы (и способны ответить на
вакцинацию) в более раннем возрасте, в то время как у других котят может быть такой высокий титр материнских антител, что они могут быть неспособны ответить на вакцинацию до возраста старше 12 недель. Группа VGG ознакомились с последними исследованиями, согласно которым до
одной трети котят могут не ответить на последнее введение базовой вакцины в возрасте 16 недель, а часть котят может все еще иметь блокирующие вакцину материнские антитела в 20-недельном возрасте (DiGangi et al. 2012, Jakel et al. 2012). Группа VGG отмечает, что одно из этих исследований было проведено на относительно небольшом количестве животных преимущественно одной породы в условиях питомника, и полагает, что эти данные могут быть не вполне применимы к
популяции кошек в целом. Тем не менее, группа VGG увеличила рекомендуемый возраст для последней вакцинации в первичной серии введения базовых вакцин с 14-16-недельного возраста до
возраста 16 недель или старше. Таким образом, рекомендации группы VGG о проведении базовой вакцинации котят согласуются с графиками, предложенными выше для щенков: начало в 6-8 недель и затем
повторение вакцинации каждые 2-4 недели до возраста 16 недель или старше. Поэтому число первичных базовых вакцинаций котенка будет определяться возрастом, когда его начали вакцинировать, и выбранным интервалом между ревакцинациями. Согласно этим рекомендациям, если начать вводить вакцины в возрасте 6 или 7 недель,
потребуется курс из четырех первоначальных введений базовых вакцин, а если начать вводить вакцины в возрасте 8 или 9 недель, то только из трех.
Неотъемлемой частью базовой вакцинации котят является ревакцинация, которая традиционно проводилась либо в возрасте 12 месяцев, либо через 12 месяцев после введения котенку последней вакцины первичной серии. Основной целью этой ревакцинации является скорее обеспечение развития защитного иммунного ответа у кошек, которые не смогли выработать иммунитет после введения какой-нибудь из вакцин первичной базовой серии, а не необходимость усилить иммунный ответ. Возраст 12 месяцев, по-видимому, исторически был выбран для введения
этой вакцины как подходящее время для того, чтобы пригласить владельца прийти на прием для первого ежегодного ветеринарного осмотра («диспансеризации»). Следовательно, в случае, если конкретный котенок не дал иммунного ответа на какую-либо из трех первичных базовых вакцинаций, он может быть не защищен вплоть до 12-месячного возраста, когда он получит следующую дозу вакцины. Этим, вероятно, объясняются случаи заболевания у некоторых вакцинированных котят в возрасте моложе 12 месяцев. Группа VGG пересмотрела такую практику
и предполагает, что ветеринарные врачи могли бы сократить это возможное окно восприимчивости путем переноса ревакцинации с 52-недельного возраста на 26-недельный (или, по сути, на любой момент времени между возрастом 26 и 52 недель; при этом 26-недельный возраст представляется удобным временем ее проведения). Для этого потребуется, чтобы владельцы домашних животных четко понимали, с чем связаны такие рекомендации, внедрение такого протокола будет означать, что вакцинация котенка, начатая в возрасте 6 или 7 недель, может повлечь за собой до пяти визитов в клинику с целью вакцинации в первые 6 месяцев его жизни. После ревакцинации базовыми вакцинами в возрасте 26 недель вводить их еще раз не потребуется как минимум в течение следующих 3 лет (для кошек с низким риском заражения). Как и для щенков, принятие метода вакцинации в возрасте 26 недель не исключает проведение первого ежегодного медицинского осмотра в возрасте 12 или 16 месяцев.
Ревакцинация взрослых кошек
Кошки, у которых выработался иммунитет в ответ на введение базовых МЖВ вакцин, сохраняют стойкий иммунитет (иммунологическую память) против FPV долгие годы без какой-либо повторной вакцинации. Иммунитет против FCV и FHV-1 является только частичным (Scott and
Geissinger 1999, Jas et al. 2015). Группа VGG рекомендует ревакцинировать взрослых кошек с низким риском заражения базовыми МЖВ вакцинами с интервалом 3 года или больше. Для кошек с высоким риском заражения ветеринарный врач может счесть целесообразным использование вакцины против FPV не чаще, чем один раз в 3 года, а вакцины против FCV и FHV-1 по-прежнему применять ежегодно, причем выбирать время их введения как можно ближе к любому очередному ежегодному размещению в зоогостинице. Эти рекомендации, как правило, не применимы ни к убитым базовым вакцинам (за исключением
бешенства), ни к дополнительным вакцинам, в особенности содержащим бактериальные антигены. Поэтому препараты, содержащие Chlamydia (ранее Chlamydophila; Sachse et al. 2015) и Bordetella, если их использование сочтено необходимым, требуют ежегодной ревакцинации для обеспечения
предоставляемой ими ограниченной защиты. Таким образом, в соответствии с этими рекомендациям, взрослую кошку по-прежнему можно ревакцинировать ежегодно, но состав используемых вакцин в разные годы будет не одинаковым. Обычной практикой в настоящее время является использование базовых вакцин (особенно против FPV) один раз в три года (с вариациями для вакцин против респираторных вирусов в зависимости от подверженности рискам) и ежегодное использование выбранных дополнительных вакцин. Группа VGG понимает, что во многих странах имеются только комплексные (ассоциированные) вакцины, сочетающие в себе базовых и дополнительных возбудителей. Группа VGG призывает производителей по возможности сделать доступным полный ассортимент вакцин повсеместно, или, как минимум, выпускать комбинацию, включающую только базовые вакцины, для тех, кто не хочет
использовать никакие дополнительные вакцины.
Взрослой кошке, которая прошла полный курс вакцинации против FPV, FHV-1 и FCV, когда она была котенком (включая ревакцинацию в возрасте 6 или 12 месяцев), но, возможно, не вакцинировалась регулярно в течение дальнейшей жизни, достаточно однократной ревакцинации базовой МЖВ вакциной для повышения иммунитета. Подобранной на улице взрослой кошке (или котенку старше 16 недель) с неизвестной историей вакцинации требуется введение лишь одной дозы базовой МЖВ вакцины против FPV для возникновения защитного иммунного ответа к этому
вирусу. И напротив, МЖВ вакцины против FHV-1/FCV для формирования полноценного иммунного ответа следует вводить подобранной на улице взрослой кошке дважды (с интервалом 2-4 недели).
Места инъекционного введения вакцин у кошек
Вакцины (любого типа) являются одним из классов инъекционных препаратов, которые связывают с патогенезом постинъекционной саркомы (саркомы на месте инъекции, Feline Injection Site Sarcoma, FISS), и особенное внимание было уделено введению адъювантных вакцин против FeLV и бешенства (Kass et al. 1993). Постинъекционная саркома была объектом многих исследований, и имеется несколько новых обзоров по этому вопросу (Martano et al. 2011, Srivastav et al. 2012, Ladlow 2013, Hartmann et al. 2015). Хотя патогенез постинъекционной саркомы остается неустановленным, в настоящее время считается, что локализованная хроническая воспалительная реакция приводит к злокачественному перерождению мезенхимальных клеток и что этот процесс имеет некоторые генетические предпосылки. Традиционным местом для большинства подкожных инъекций (включая вакцины) у кошек была межлопаточная область, где часто образуется постинъекционная
саркома. Из-за инфильтративной природы этих опухолей для их удаления часто бывает необходима радикальная хирургическая резекция (иссечение), хотя применяются и дополнительные методы
лечения (Martano et al. 2011, Ladlow 2013). В Северной Америке с учетом этой проблемы было рекомендовано вводить две адъювантные вакцины, считающиеся высокорискованными, в определенные анатомические места, откуда будет проще удалить постинъекционную саркому в случае ее возникновения. Рекомендация «левая задняя конечность – лейкемия, правая задняя конечность – бешенство» (left leg leukaemia, right leg
rabies) означала, что вакцину против FeLV следует вводить в дистальную часть левой тазовой конечности, а вакцину против бешенства – в дистальную часть правой. Эта рекомендация до сих пор включена в руководство Американской ассоциации практикующих врачей-фелинологов (AAFP) (Scherk et al. 2013), которое также предписывает вводить три базовые вакцины для кошек в дистальную часть передней конечности. Было проведено одно исследование, в котором оценивали
эффект такой практики путем сравнения анатомического расположения постинъекционной саркомы у кошек до принятия данной рекомендации (1990-1996) и после ее реализации на практике (1997-2006) (Shaw et al. 2009). Результаты показали, что случаев образования постинъекционной саркомы в межлопаточной области стало значительно меньше, а случаев образования опухолей на правой (но не на левой) тазовой конечности – больше. Более того, увеличилось число сообщений об опухолях, захватывающих одновременно правую заднюю конечность и правую латеральную (боковую) поверхность живота (12,5% — 25,0%) или левую заднюю конечность и левую латеральную поверхность живота (11,4% — 13,8%). Это было объяснено случайным попаданием препаратов в эти
абдоминальные области при проведении неудобных для выполняющего их человека инъекций в дистальные части задних конечностей. За пределами Северной Америки эта практика не получила широкого распространения. В одной из недавних публикаций была показана действенность введения вакцин против FPV и бешенства кошкам в хвост (Hendricks et al. 2014). Взрослые кошки-участницы программы «отловстерилизация-возврат» получали инъекцию трехкомпонентной базовой МЖВ вакцины (FPV, FHV1, FCV) в дистальную треть дорсальной поверхности хвоста, а инактивированную вакцину против бешенства им вводили на 2 см дистальнее (ниже) места введения трехкомпонентной вакцины. Сероконверсия отмечалась у всех кошек для FPV и у всех кроме одной для вируса бешенства. В этом небольшом исследовании сообщалось, что вакцинация в хвост хорошо переносилась кошками. В Руководстве WSAVA по вакцинации собак и кошек 2010 года группа VGG предложила
альтернативный вариант введения вакцины – под кожу латеральной части грудной клетки или, еще лучше, латеральной части живота (Day et al. 2010). Инъекция в хвост может оказаться более безопасной альтернативой, чем инъекции в дистальную часть конечности либо латеральную поверхность тела, но потребуются дальнейшие исследования такого способа введения вакцин. Этот вопрос остается спорным и неоднозначным, и каждый практикующий ветеринарный врач должен решить для себя, какой из подходов является удобным для применения в условиях его клиники. Тем не менее, необходимо придерживаться следующих принципов:
Польза защитного иммунитета, обеспечиваемого вакцинами, перевешивает любой риск развития постинъекционной саркомы. По современным оценкам, распространенность постинъекционных сарком составляет 1 на каждые 5 000-12 500 вакцинированных кошек (Gobar and Kass 2002, Dean et al. 2013).
По возможности следует использовать для кошек неадъювантные вакцины.
Вакцины (особенно адъювантные) или другие инъекционные препараты не следует вводить в межлопаточную область.
Вакцины (особенно адъювантные) следует вводить в другие места подкожно (а не внутримышечно). Места для введения следует выбирать, руководствуясь балансом между простотой хирургической резекции постинъекционной саркомы в случае ее возникновения и приемлемым уровнем безопасности для вакцинирующего (т.е. необходимо избегать случайного самовведения вакцины при фиксации сопротивляющегося животного).
Каждый раз вакцины следует вводить в разные места. Место введения следует помечать на рисунке в истории болезни или вакцинационном паспорте пациента, указывая там же, какие именно вакцины были введены в каждом конкретном случае. Mеста введения вакцины следует
чередовать. В качестве альтернативного варианта в рамках клиники можно выбирать единое место введения всех вакцин кошкам всеми сотрудниками в течение данного календарного года и менять
его на следующий год.
Группа VGG призывает сообщать обо всех случаях подозрений на постинъекционные саркомы по соответствующим национальным каналам, предусмотренным для уведомлений о предполагаемых побочных эффектах, или отправлять уведомления напрямую производителям вакцин.
Серологическое тестирование
Со времени публикации Руководства 2010 года стал доступным один коммерческий быстрый тест для определения в сыворотке крови антител к FPV, FCV и FHV-1, предназначенный для применения в клиниках (экспресс-тест). Он уже сертифицирован и был использован в серии опубликованных научных исследований (DiGangi et al. 2011, Mende et al. 2014) [EB1]. Этот экспресс-тест может использоваться для определения наличия защитных антител против FPV, поскольку существует превосходная корреляция между присутствием таких антител и устойчивостью к заражению (Lappin et al. 2002) [EB1]. Сообщается, что в отношении FPV тест имеет специфичность 89% и чувствительность 79% (Mende et al. 2014) либо специфичность 99% и чувствительность 49%
(DiGangi et al. 2011) при сравнении с реакцией задержки гемагглютинации. Отрицательный результат теста означает, что антител у кошки мало или они отсутствуют, поэтому рекомендуется ее ревакцинировать. Но некоторые серонегативные кошки на самом деле имеют иммунитет
(результат ложноотрицательный), и их ревакцинация была бы излишней. Напротив, положительный результат теста должен привести к заключению о том, что ревакцинация не требуется. Корреляция между циркулирующими в крови антителами и защитой против заражения FCV
и FHV-1 менее надежна, чем наличие адекватной местной иммунной защиты слизистых оболочек и клеточного иммунитета. По этой причине отрицательный результат теста для определения антител к FCV и FHV-1 не всегда означает отсутствие защиты у данной кошки (Lappin et al. 2002).
Эти тесты могут применяться на практике как описано выше для собак: для определения защиты у котят после вакцинации против FPV, для определения защиты взрослых кошек от FPV (для обоснования решений о ревакцинации) и для использования в условиях приютов для контроля
вспышек FPV-инфекции. Следует подчеркнуть, что тестирование на антитела к FIV используется для диагностики болезни и не имеет никакой ценности для определения иммунитета к FIV, но, как
говорилось выше, когда используется вакцина против FIV и предполагается инфицирование FIV, диагноз следует ставить с помощью селективного (дискриминационного) серологического теста либо, что предпочтительнее, валидизированного (одобренного) ПЦР-теста.
